日前,健康元藥業集團股份有限公司發布公告稱,其控股子公司麗珠集團控股附屬公司麗珠試劑自主研發的新型冠狀病毒抗原檢測試劑盒獲國家藥品監督管理局批準注冊上市,該新冠抗原檢測試劑盒適用于鼻咽拭子,口咽拭子,鼻拭子三種樣本類型,檢測時間僅需15分鐘,操作簡單,結果清晰,易于判讀,無需實驗室,可用于自測。
在當前Omicron傳播迅速的情況下,按照流行病學防控要求,快速識別傳染源,需要更加簡便,易行并且容易推廣的檢測技術,以適應當下毒株的流行特征,從而應對更多的人群開展大規模快速檢測目前市場上,已取得注冊證的自測抗原試劑方法學分別有熒光免疫層析法,膠體金法和乳膠法其中,熒光免疫層析法是需要額外的設備配合判讀的,自測的時候基本無法使用,而膠體金法和乳膠法是不需要儀器可以自己檢測的
據介紹,麗珠試劑自研的新型冠狀病毒抗原檢測試劑盒在檢測上比膠體金法更具優勢:一方面,采用彩色乳膠微球粒作為信號標記,乳膠微球粒徑均一,且比常規膠體金顆粒大5—10倍,則乳膠法在檢測靈敏度上有所提高,另一方面,彩色乳膠微球合成時摻入了羧基等活化基團,標記抗體與乳膠通過化學鍵共價連接,所以比膠體金與蛋白之間通過電荷連接更穩定。
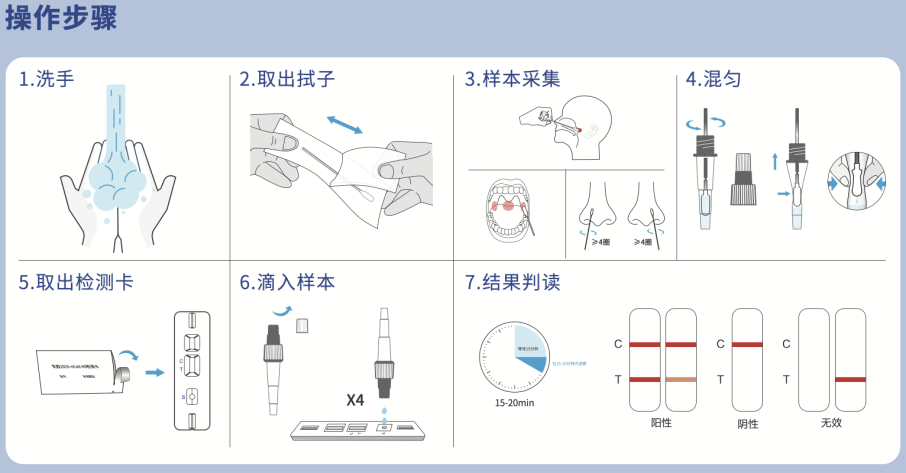
從具體優勢來看,該產品簡便易行,無需任何儀器設備就可進行快速自我檢測,在15—20分鐘內獲取檢測結果,該產品設計友好,提供了適用鼻咽拭子,口咽拭子,鼻拭子,以及1人份/盒,5人份/盒,20人份/盒的多樣本類型,多規格及組分設計,可以滿足不同場景需求。
 更重要的是,該產品在臨床試驗中采用了國內人群的數據驗證,更貼合當前國內情況,使得結果更可靠。2021年5月17日,廣東省醫療保障局,廣東省衛生健康委員會,廣東省藥品監督管理局聯合發布《關于做好我省新型冠狀病毒檢測試劑采購和使用工作的通知》,正式落地此次集采。
日前,國家衛生健康委員會發出《新冠病毒抗原檢測應用方案》,首次提出在核酸檢測基礎上,增加抗原檢測作為補充鑒于此,麗珠試劑根據政策加快相關工作,在珠海市委,市政府,香洲區委,區政府,藥監等各級部門的指導下,以最快的速度完成注冊資料的準備,并于3月29日向國家藥品監督管理局提交了注冊申請,4月12日取得注冊證抗原檢測試劑盒,注冊證號:國械注準20223400470)在此之前,麗珠試劑新冠抗原試劑盒已獲得歐盟CE,英國,印尼和泰國注冊證,以及法國,德國,奧地利等國家和地區的白名單準入資格,產品銷往歐盟,亞太等多個國家和地區
麗珠試劑新型冠狀病毒抗原檢測試劑盒用于體外定性檢測新型冠狀病毒N蛋白抗原,可以應用于醫療機構,也可在隔離人員,密接人員,有自我檢測需求的社區居民中進行自我檢測,有效緩解國內檢測壓力,對新冠病毒感染早期檢測具有重要意義。。
。鄭重聲明:此文內容為本網站轉載企業宣傳資訊,目的在于傳播更多信息,與本站立場無關。僅供讀者參考,并請自行核實相關內容。
|
